暮らしのなかの身近な放射線
7
放射線の具体的な利用例
その1. (強い)放射線でモノの性質を変える!❸分子を切る(切断)
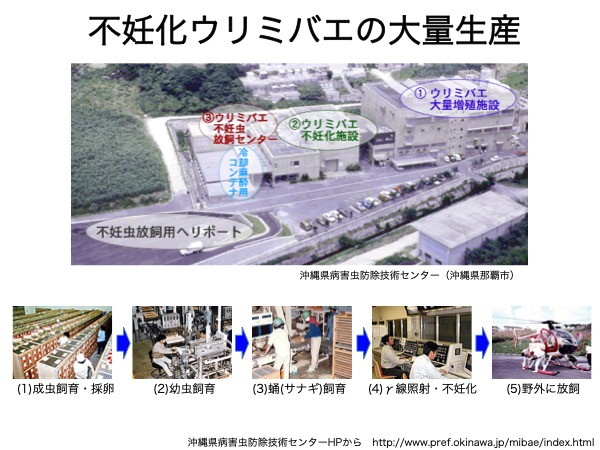
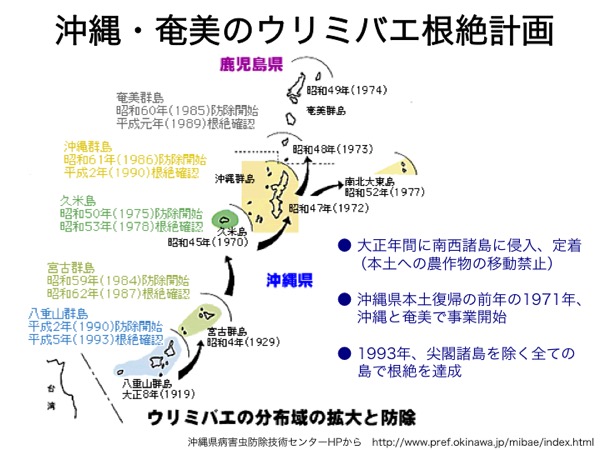
③不妊虫放飼法による野外の害虫根絶(不妊化)
不妊虫放飼法とは、防除対象の虫を人工的に大量飼育し、放射線照射で不妊化したのちに野外に大量に放ち、野生虫同士の繁殖機会を奪って次世代の個体数を減少させ、ついには根絶に導く方法である南西諸島で実施されている不妊虫放飼法におけるウリミバエやアリモドキゾウムシの不妊化は60〜70 Gyで達成できる。




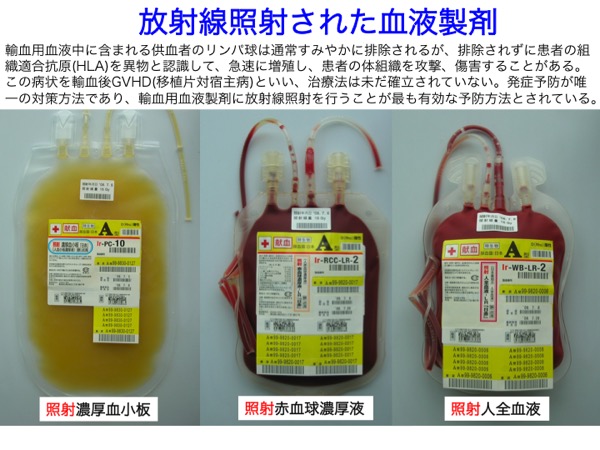
④輸血用血液製剤のリンパ球不活性化
一般にはあまり知られていない利用法に、輸血用血液製剤の照射処理がある。日本では、他人血から作られた血液製剤による輸血後移植片対宿主病予防のために15〜50 Gyの放射線照射が義務づけられている。15 Gyはリンパ球の不活性化に必要な線量で、50 Gyは赤血球や血小板が劣化しない上限線量である。

⑤がん治療(がん細胞の致死、増殖抑制)
一般的な放射線がん治療では、電子加速器(リニアック)で発生させたX線を1回あたり2 Gy程度で繰り返し照射する。他に、Co-60線源のγ線をヘルメット型のコリメータを通して201本の細いビームとして体内の一点に収束させ、病変部をピンポイントで集中照射して治療する定位放射線治療装置があり、開頭手術をせずに脳深部の病巣をナイフで切り取るように治療できることから「ガンマナイフ」と呼ばれている。
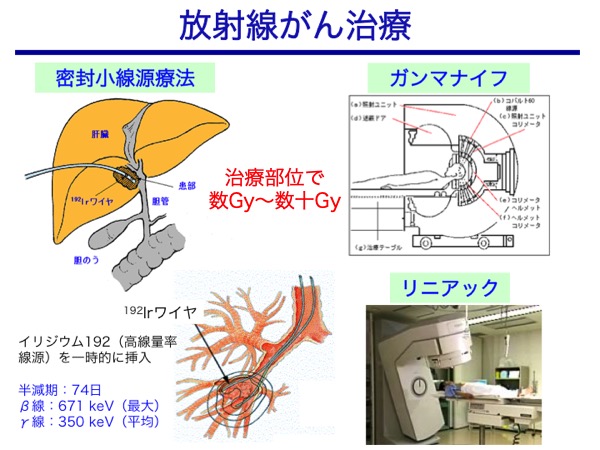

体外からの照射の他に、小さな容器に密封されたRIを用いる密封小線源療法として、子宮や気管支などの腔内照射(Co-60、Ir−192)、病変組織に刺入した細い管を通して密封小線源(Ir−192、I-125、Au-198)を挿入する組織内照射、低線量率のカプセル線源(I-125)を患部に永久刺入(留置)する前立腺がん治療などがある。さらに、RI(または放射性RI標識薬剤)そのものを体内に静注あるいは経口投与するRI内用療法として、I-131による甲状腺がんや転移巣の治療、Sr-89による骨転移がんの治療や疼痛緩和、Y-90やIn-111で標識したモノクローナル抗体によるリンパ腫の放射免疫療法があり、最近ではRa−223やAt−211などのα線放出核種による治療や臨床試験に向けた研究が始まっている。
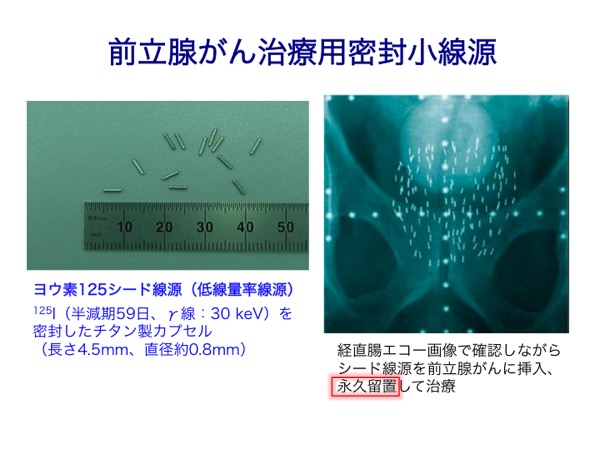

RI内用療法では、患部だけが局所的に照射されるように飛程が短いβ線やα線が主に用いられるが、I-131などγ線も放出する核種の場合にはその薬剤の患部への集積を体外からモニターすることも行われている。
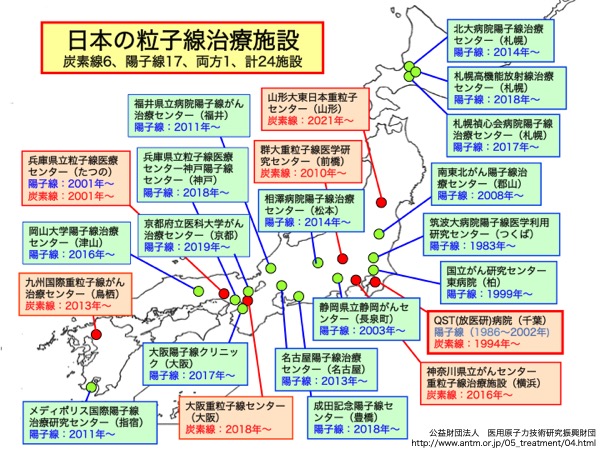
最近普及しつつある重粒子線(炭素線)がん治療は、腫瘍部への線量集中性が高いだけでなく、X線に抵抗性のがんにも有効な点が優れている。一度に大きな線量を照射し、より少ない回数で、究極的には1回だけの照射による治療を目指しており、仕事を続けながら治療ができるメリットは大きい。
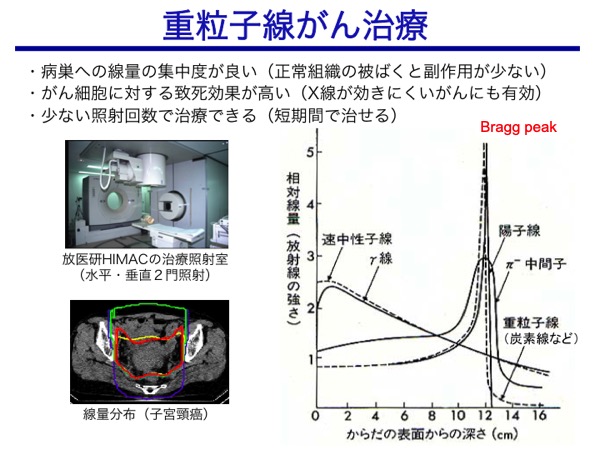

一方、陽子線(水素イオンビーム)がん治療は、生物効果の点ではX線と同等であるが、重粒子線(炭素線)と同等の腫瘍部への線量集中性の高さを、よりコンパクトな加速器で実現できるため、炭素線がん治療施設との使い分けが図られている。
いずれの場合も、がん組織と正常組織の放射線傷害からの回復力の違いを最大限に利用し、重篤な副作用を防ぎながらがんを制御するために、線量と照射間隔の最適化や薬剤の併用などが模索されている。

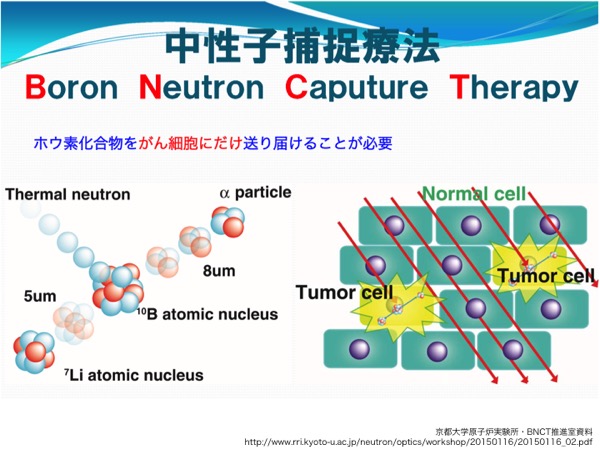
悪性脳腫瘍など、輪郭がはっきりしないため体外からの照射による治療が有効でない浸潤性のがんに対しては、BNCT(Boron Neutron Capture Therapy, ホウ素中性子捕捉療法)が切り札となる。ホウ素の安定同位体B-10をがん細胞に選択的に取り込ませた後に、体外から熱中性子(速度の遅い中性子)を照射すると、がん細胞内で熱中性子がB-10原子核に吸収されて核反応を起こし、He-4(α線)とLi-7(反跳核)に分裂して反対方向に放出される。両者の飛程はほぼ細胞のサイズであるため、そのがん細胞だけが死滅することになる。B-10を取り込んでいない細胞に対しては、熱中性子の多くは透過するだけで、ほとんど影響を与えない。(ごく一部の熱中性子は窒素14と反応して炭素14に変わり、その際に放出された陽子が周囲に線量を与える)